El desorden impulsa una de las máquinas más complejas de la naturaleza
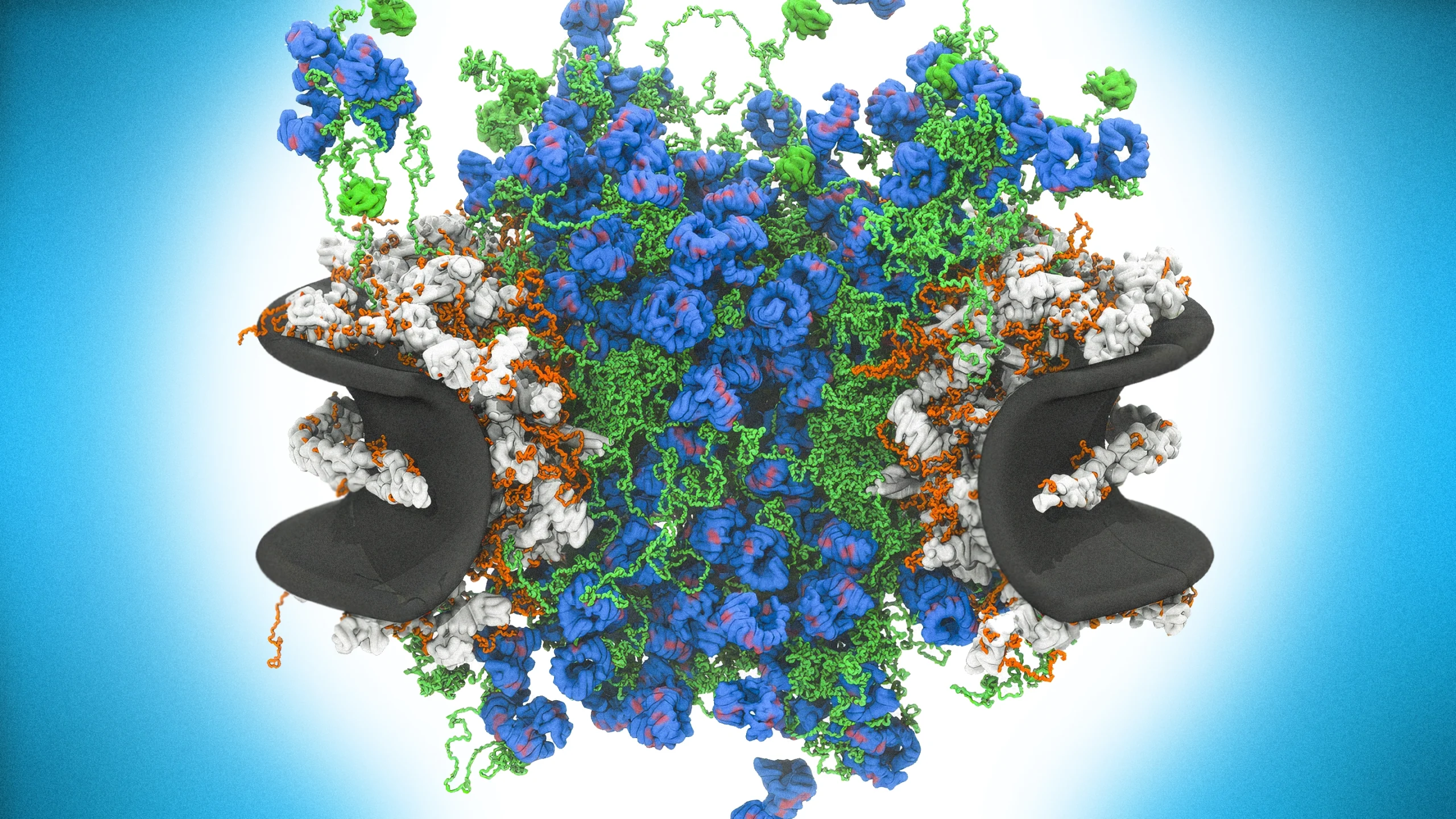
El canal interno del complejo del poro nuclear en todo su esplendor. Lejos de ser un simple poro, este complejo está repleto de proteínas dinámicas que transportan moléculas dentro y fuera del núcleo. En este modelo computacional, las hebras verdes representan proteínas nucleoporinas desordenadas y los nudos azules, proteínas transportadoras de carioferina.
Introducción
En los albores de la vida compleja, la evolución creó un contenedor para el ADN, su objeto más preciado. Unos miles de millones de años después, los microscopistas del siglo XX observaron de cerca este contenedor —el núcleo— y vieron que estaba cubierto de diminutas aberturas. En aquel entonces, no sabían qué interpretar de estas estructuras, pero a medida que la microscopía mejoraba, algo grandioso se hizo evidente: lo que ahora llamamos «complejos de poros nucleares», algunas de las máquinas moleculares más grandes y maravillosas jamás formadas.
Cada complejo de poros nucleares está formado por cientos de proteínas, de unos 30 tipos diferentes. De frente, parece una flor de ocho pétalos; de perfil, un platillo volante. Su abertura central rebosa de proteínas con forma de espagueti, unidas a las paredes internas del complejo.
“Es una cosa de enorme belleza”, dijo Brian Chait., biólogo químico de la Universidad Rockefeller. «Es maravilloso. Es una maravilla. Es fenomenal».
Esta máquina tiene una función vital: dirigir el tráfico molecular hacia dentro y hacia fuera del núcleo. Más que una puerta abierta, el complejo proteico reconoce las diferentes moléculas a medida que se acercan y solo deja pasar a algunas. «El complejo del poro nuclear es, en última instancia, el guardián del núcleo», afirmó Roderick Lim., biofísico de la Universidad de Basilea, Suiza. «Todo lo que entra y sale del núcleo debe pasar por estos poros».
Casi todas las células eucariotas tienen un núcleo perforado por complejos de poros nucleares, y los componentes principales de este complejo se conservan increíblemente bien en todas las especies, desde las levaduras unicelulares hasta los humanos multicelulares. La evolución «se inventó algo una vez y se quedó atascada con él», dijo André Hoelz., biólogo celular estructural del Instituto de Tecnología de California.
Un solo núcleo de mamífero puede contener miles de ellos. Cada segundo, cada poro nuclear deja pasar de cientos a miles de moléculas de todas las formas y tamaños para que puedan viajar a sus destinos y producir proteínas, regular genes y, en general, contribuir al funcionamiento celular. Algunas moléculas grandes son transportadas a través del canal por proteínas, mientras que las pequeñas se difunden por sí solas. Y mientras algunas se deslizan sin esfuerzo, para otras es una barrera impenetrable.
Cómo funciona esta puerta con tanta selectividad es un misterio. Durante décadas, los biólogos han descifrado el aspecto de la mayoría de las partes estáticas de la máquina. Pero su centro es inquieto, en constante movimiento y transformación, lo que dificulta su visualización incluso con los mejores métodos.
Eso está cambiando gradualmente. En un estudio publicado en Nature Cell BiologyA finales de 2025, la microscopía de alta resolución mostró la barrera central en movimiento con una resolución de milisegundos, revelando una estructura flexible que se reorganiza constantemente. Las imágenes experimentales, respaldadas por modelado computacional,, sugiere que la función del complejo de poro nuclear está guiada por la flexibilidad y el movimiento.
Esto es más que una simple curiosidad intelectual. Un auge de investigaciones recientes ha vinculado los trastornos del desarrollo neurológico, las enfermedades virales y los cánceres con problemas en este complejo. Si los biólogos logran discernir cómo funciona su sistema de tráfico celular, podrían desarrollar métodos para impedir el paso de patógenos indeseados, e incluso intentar guiar moléculas terapéuticas hacia el núcleo celular, donde aguarda el genoma.
“Estamos empezando a acercarnos a una imagen casi atómica de los poros nucleares de varios organismos”, dijo Mike Rout., biólogo celular de la Universidad Rockefeller que dirigió el nuevo trabajo que ofrece información sobre una máquina molecular en el corazón de la vida eucariota.
Una cosa de belleza
Para muchos científicos que estudian el poro nuclear, fue una fascinación instantánea: estaban asombrados de que esta máquina biológica (relativamente) masiva pudiera permitir que tantos tipos de moléculas, y tantas de ellas, entraran y salieran del núcleo de manera eficiente, con poco margen de error.
"Es precioso", dijo Hoelz. "¿Cómo se crea un hangar con una puerta por la que pueda pasar un 747, pero que no pueda salir volando una canica pequeña?"
De alguna manera, la propia puerta debe actuar como portero para las moléculas importantes de la vida. Las moléculas de ARN deben salir del núcleo hacia el citoplasma para producir proteínas. Los ribosomas, las estructuras encargadas de la síntesis de proteínas, están compuestos por moléculas ensambladas en el núcleo y expulsadas a través de los poros. Mientras tanto, las moléculas implicadas en la regulación del genoma deben ser introducidas preferentemente en el núcleo. A medida que estos procesos se desarrollan, el poro nuclear también bloquea elementos no pertenecientes a su lugar, como enzimas dañinas o ARN mal plegados.

El biólogo celular Mike Rout ha dedicado décadas al estudio del complejo del poro nuclear. Esta estructura vital, formada por cientos de proteínas individuales, es el guardián y controlador del tráfico del núcleo celular.
Lori Chertoff/Universidad Rockefeller
En las décadas transcurridas desde el descubrimiento del complejo de poros nucleares, los biólogos han ido adquiriendo una mayor comprensión de su estructura mediante la microscopía electrónica, herramientas físicas y modelado computacional. Con la llegada de la criomicroscopía electrónica, una potente técnica que permite obtener imágenes de las células tras su congelación instantánea, han podido evaluar las partes estáticas de la máquina.Estos esfuerzos han generado una visión casi atómica de cada proteína individual que construye las ocho unidades radiales con forma de pétalo. Sin embargo, la técnica no ha funcionado para el centro, llamado canal de transporte, donde ocurre la mayor parte de la acción del poro.
“Cada vez que alguien usa alguno de estos microscopios para observar el interior de los poros nucleares, solo ve una nube amorfa en su interior”, dijo Lim. “Es como una neblina”.
La razón, que se hizo evidente en la década de 1990, es que el centro de esta gigantesca máquina está lleno de proteínas sin una estructura obvia ni específica. Estas proteínas, llamadas FG-nucleoporinas, tienen colas que se mueven como algas y que no pueden captarse en imágenes estáticas. Estas colas son «la materia oscura del complejo de poros nucleares», explicó Hoelz.
La mayoría de las proteínas se pliegan en estructuras o formas específicas esenciales para las funciones que desempeñan en la célula. Pero las proteínas intrínsecamente desordenadas , una categoría que incluye estas nucleoporinas, carecen de una estructura única. Se mueven, cambiando de forma y uniéndose a diferentes moléculas.
Esto significa que en el centro del complejo de poros nucleares, “todo está mediado por el desorden”, dijo Patrick Onck., físico computacional de la Universidad de Groningen, Países Bajos. «No es el orden lo que genera esta función. Es el desorden».
A principios de la década de 2000, el campo estaba inmerso en debates sobre la organización y el comportamiento de las nucleoporinas FG en el canal de transporte y cómo podrían transportar moléculas dentro y fuera del núcleo. Los investigadores coincidían en que la mayoría de las macromoléculas no pueden atravesar el canal sin la ayuda de proteínas transportadoras llamadas factores de transporte. Estos factores, que se mezclan con las nucleoporinas en el canal, se unen únicamente a aquellas moléculas que incluyen una secuencia corta específica de aminoácidos: una etiqueta molecular que, en efecto, indica "envíenme al núcleo", explicó Rout. Sin embargo, los investigadores discrepaban sobre cómo podría estar organizado el propio canal, lo que influiría en el movimiento de las moléculas a través de él. Algunos argumentaban que las nucleoporinas se acoplan entre sí, formando una red de malla similar a un gel. Otros sostenían que las proteínas desordenadas no interactúan mucho entre sí, sino que ondulan constantemente como las cerdas de un pincel.
El debate se tornó polémico. «Antes era muy hostil», recordó Hoelz. «La gente siente mucha pasión por lo que hace. No se trata de una animosidad personal».
“Durante mucho tiempo, la pregunta era: '¿Eres de gel o de pincel?' O eres de uno u otro”, dijo Siegfried Musser., bióloga celular en la Universidad de Texas A&M.

El biofísico Roderick Lim y su equipo utilizaron microscopía de fuerza atómica de alta velocidad para obtener imágenes del funcionamiento interno del complejo del poro nuclear.
Biozentrum, Universidad de Basilea
En los últimos años, nuevas colaboraciones y debates, incluyendo una conferencia anual donde los principales actores se reúnen para conversar, han apaciguado el conflicto. Sin embargo, la verdad sobre la estructura y el funcionamiento del canal de transporte aún no se había resuelto. Los investigadores tendrían que ser más creativos para comprender cómo funciona el complejo en su entorno natural.
“Simplemente queríamos volver al complejo del poro nuclear y pedirle al poro nuclear que nos dijera qué está haciendo”, dijo Rout, “no imponerle lo que está haciendo”.
Golpeador rápido
¿Cómo se interroga un complejo molecular? Rout y Lim, quienes han defendido un modelo más dinámico del poro nuclear, comenzaron con una idea simple: pincharlo.
Rout ha dedicado décadas a caracterizar los complejos de poros de la levadura. Lim es un experto en microscopía de fuerza atómica de alta velocidad, una técnica que consiste en deslizar una sonda muy afilada sobre una superficie, golpeándola suave y rápidamente, para comprender cómo se mueve.
Hace unos años, en un oscuro laboratorio en un sótano, el estudiante de posgrado de Lim, Toshiya KozaiComenzó a desempaquetar viales de plástico que contenían millones de complejos de poros nucleares de levadura. Trabajó sin descanso durante días en el “cuarto sótano de nuestro departamento”, recordó Lim, para introducir las muestras en el microscopio de fuerza atómica de alta velocidad mientras aún estaban frescas. “Es un verdadero trabajo de amor”.
Sus esfuerzos permitieron al equipo observar cómo cambiaba el canal de transporte, milisegundo a milisegundo. «Pudimos ver un movimiento muy nítido y ultrarrápido», recordó Rout. Los vídeos resultantes pueden parecer borrosos para nosotros, seres macroscópicos, pero representan algunas de las imágenes de mayor definición del comportamiento del canal de transporte nanoscópico.
En los bordes del canal, cerca de las paredes, el equipo de Rout y Lim observó rápidas fluctuaciones de moléculas: se trataba de las nucleoporinas, que se movían de forma ondulante. En el centro, vieron una masa difusa, conocida como tapón central, que se desplazaba y reposicionaba continuamente dentro del canal de transporte. Durante mucho tiempo, los biólogos habían sospechado la existencia de un tapón central, pero en imágenes de microscopía anteriores no siempre era visible.
“Ver para creer”, dijo Hoelz, quien no participó en el estudio. Poder demostrar esto “es algo maravilloso”.
Dirigido por Chait y utilizando espectrometría de masas, el equipo descubrió que el tapón estaba formado por proteínas de transporte llamadas carioferinas, o "kaps" para abreviar, además de su carga molecular. A medida que las kaps se mueven a través del poro nuclear, se adhieren a las nucleoporinas, atrayéndolas hacia el centro del canal. Esto crea un obstáculo dinámico y temporal que ralentiza otras moléculas o les impide el paso. De esta manera, las kaps no solo ayudan a transportar moléculas, sino que también repelen todo lo que no debería estar allí, explicó Rout. Cuando añadieron más factores de transporte, observaron que el tapón aumentaba de tamaño.
El núcleo del complejo del poro nuclear se reorganiza constantemente mediante la acción de las proteínas kap, creando un entorno en constante cambio. Los resultados sugieren que la organización y el comportamiento del poro son mucho más dinámicos que una red de gel, explicó Rout, y mucho más similares a un entorno con forma de cepillo. Estos hallazgos respaldan un modelo que propuso anteriormente, denominado "puerta virtual", en el que la dinámica del entorno es crucial para dirigir las proteínas hacia afuera o a través de él. Lo comparó con una pista de baile abarrotada.
“Si sabes bailar, puedes simplemente entrar al baile y pasar de una pareja a otra, tomados de la mano, intercambiando rápidamente”, dijo. “Si no sabes bailar, lo único que ves es un caos, y tratas de unirte. Nadie te sujeta para ayudarte a entrar al baile, así que simplemente te empujan”.
Para poner a prueba sus observaciones, Rout y Lim crearon poros sintéticos del mismo tamaño que los complejos de poros nucleares naturales. Al anclar nucleoporinas en su interior y añadir factores de transporte, los poros sintéticos se comportaron como los complejos de poros nucleares de la levadura silvestre. Observaron la aparición del tapón central.
“Lo que me resulta realmente sorprendente es que reproducen el resultado con un modelo muy simple”, dijo Musser. “Es un resultado asombroso”.
Puerta no cerrada
Hoelz no está del todo convencido de que esto suponga el fin definitivo del modelo de gel. «La respuesta probablemente se encuentre en un punto intermedio, como suele ocurrir en ciencia», afirmó. Sugirió que es probable que los investigadores observen el canal central en diferentes configuraciones debido a su constante cambio, o quizás los canales internos de algunos poros nucleares se asemejan más a un gel y otros a un pincel.
Un estudio de modelización reciente dirigido por Onck y publicado en Nature CommunicationsSe sugirió que el canal de transporte central podría tener partes con estructura de cepillo y otras similares a condensados : compartimentos líquidos sin membrana con características de geles y cepillos. Incluso podría darse el caso de que el centro más denso del canal tuviera cualidades más parecidas a un gel o condensado, explicó Musser, mientras que la periferia se asemejara más a un cepillo.
Hoelz afirmó que solo las nuevas tecnologías que permitan ver completamente el interior del poro resolverán el debate, y que podrían llegar en cualquier momento.
“La gente intenta constantemente desarrollar nuevas herramientas o nuevas estrategias para intentar comprender lo que está sucediendo”, coincidió Musser. En 2025, él y su equipo publicaron los resultados en Nature.que utilizó una potente herramienta de imágenes 3D llamada Minflux para rastrear moléculas en alta resolución mientras se mueven a través de los complejos de poros nucleares en núcleos intactos de células humanas. Conocer este método fue "un cambio radical para mí", dijo Hoelz, quien no participó en el estudio.
El equipo de Musser observó que las moléculas se movían únicamente cerca del borde del canal de transporte. Esto complementa el estudio de Rout y Lim, dado que el tapón central podría estar bloqueando el centro. «Pero no tiene sentido que el centro no se utilice», dijo Musser. «Creo que simplemente no hemos encontrado el sustrato adecuado ni desarrollado las herramientas necesarias para observar el paso de las sustancias por el centro».
Independientemente de su aspecto interno, es evidente que el complejo del poro nuclear es increíblemente maleable y robusto, lo que también lo convierte en el "talón de Aquiles" de la célula, según Rout. Es fundamental para la salud celular y fundamental para sus procesos más importantes: la producción de proteínas y la regulación génica. Pero, gracias a su resiliencia y a su capacidad para soportar daños, puede verse alterado por enfermedades sin inutilizarse.
Algunas proteínas que componen el poro nuclear "aparecen una y otra vez como puntos débiles para las enfermedades", afirmó Rout, incluyendo trastornos del neurodesarrollo, enfermedades virales y cánceres. Tanto las células cancerosas como los virus...Probablemente interfieran con las proteínas del complejo para inclinar la maquinaria de producción de proteínas a su favor o desactivar una respuesta inmune.
En ese sentido, el complejo de poros nucleares es mucho más que una puerta molecular. «Es un nexo para la integración de la información», dijo Rout. «Y creo que si la célula tuviera pensamientos, así es como pensaría en sus poros nucleares».

